بررسی جامع ترکیبات یونی خواص و ویژگی های آنها
می دانید که طبقه بندی پیوندهای شیمیایی در شیمی به صورت دو دسته اصلی پیوندهای یونی وکوالانسی است و انواع دیگر پیوند مانند پیوند کوالانسی قطبی و هیدروژنی و یا پیوند فلزی در رده های دیگر پیوند های شیمیایی قرار می گیرد.
يونهاي تک اتمي:
به هر يوني که از يک اتم آن هم بر اثر گرفتن يا از دست دادن يک يا چند الکترون تشکيل مي شود يون تک اتمي مي گويند.
فلزهاي گروه اول با از دست دادن يک الکترون تبديل به کاتيون با بار +۱ ميشوند مثل Na+
فلزهاي گروه دوم ، با از دست دادن دو الکترون تبديل به کاتيون ۲+ مي شوند مثل ۲+ Mg
نافلزهاي گروه ۶۱ با گرفتن دو الکترون به آنيوني با بار ۲- تبديل مي شوند مثل ۲- O
نافلزهاي گروه ۷۱ با گرفتن دو الکترون به آنيوني با بار ۱- تبديل ميشوند مثل Cl-
بعضي فلزهاي واسطه بدون داشتن آرايش الکتروني گاز نجيب به پايداري مي رسند. برخي از اين عنصرها مي توانند يونهايي با بار متفاوت داشته باشند مثل
+۲ Fe و ۲+ Fe يا ۳+ Mn و۳+ Mn
اين يونها را به ترتيب يون را به ترتيب آهن (II ) و يون آهن (III) يا يون منگنز (II) و يون منگنز (III) مي نامند.
ماهیت یون:
وقتی اتمها به یون تبدیل میشوند، خواص آنها شدیدا تغییر می کند. مثلاً مجموعهای از مولکولهای برم قرمز است. اما یونهای برم در رنگ بلور مادهٔ مرکب هیچ دخالتی ندارند. یک قطعه سدیم شامل اتمهای سدیم نرم است. خواص فلزی دارد و بر آب به شدت اثر میکند. اما یونهای سدیم در آب پایدارند.
مجموعه بزرگی از مولکولهای کلر، گازی سمّی بهرنگ زرد مایل به سبز است، ولی یونهای کلرید مواد مرکب رنگ ایجاد نمیکنند و سمّی نیستند. به همین لحاظ است که یونهای سدیم و کلر را به صورت نمک طعام میتوان بدون ترس از واکنش شدید روی گوجه فرنگی ریخت. وقتی اتمها به صورت یون در میآیند، ماهیت آنها آشکارا تغییر میکند.
در زیر می خواهیم به خواصی که پیوندهای یونی از خود نشان می دهند، اشاره کنیم.
دمای ذوب: ترکیبات یونی، دمای ذوب نسبتا بالایی دارند. حتی یک نمک معمولی خانگی (NaCl)، دمای ذوبی در حدود 700 درجه سانتی گراد دارد.
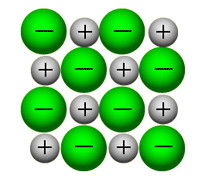
بلور (کریستال) یک ترکیب یونی توسط نیروهای بسیار قوی الکتروستاتیکی، استحکام خود را حفظ می کند، در این حالت، یون های مثبت و منفی همدیگر را جذب می کنند.
یون ها به راحتی در حالت جامد بلور ارتعاش می کنند و زمانی که به بلور یونی، گرما می دهیم تا ذوب شود، این یون ها به راحتی جریان پیدا می کنند.
همان گونه که در شکل سمت راست نیز دیده می شود، یون ها در بلور یونی به صورت بسیار نزدیک و پکیده در کنار هم توسط نیروهای الکتروستاتیکی قرار گرفته اند و برای مثال در بلور NaCl، هر یون با 6 یون با بار مخالف خود احاطه شده است.
در حالت ذوب شده، یون هایی که آزادانه حرکت می کنند، می توانند یک جریان الکتریکی را از طریق خود، هدایت کنند. در حالی که در حالت جامد همین بلور یونی، مکان ثابت و آرایش بسیار کیپ یون ها اجازه هدایت جریان الکتریسیته را نمی دهد.
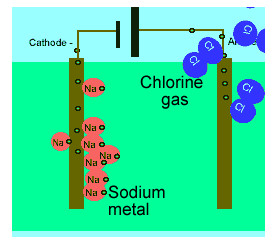
برای این که ببینید ترکیبات ذوب شده یونی چگونه الکتریسیته را هدایت می کنند، شکل زیر را در مورد الکترولیز نمک طعام ذوب شده ببینید.
باید بدانید که نیروهای الکتروستاتیکی در شبکه بلوری، در جهت های بسیار ویژه عمل می کنند و همین باعث می شود، ترکیبات یونی بسیار شکننده باشند.
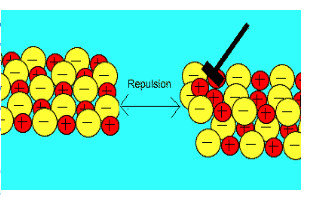
زمانی که یک نیرو به یون های بلور یونی (که یون های آن با بارهای مخالف در کنار هم قرار گرفته اند) اعمال می کنیم (مثلا چکش بر آن فرود می آید)، این یون ها از خط و آرایش قبلی خود خارج شده و نزدیک یون هایی با بار مشابه خودشان قرار می گیرند؛
بنابراین
اکنون نیروی دافعه است که باعث از هم پاشیده شدن شبکه یونی با اعمال یک نیرو (مثل چکش) می شود.
بیش تر ترکیبات یونی، قابل انحلال در آب هستند. در محلول آبی، به دلیل خاصیت از هم جدا کنندگی مولکول های آب، بارهای ترکیب یونی از هم جدا می شوند.
مولکول های آب با مختصر باری که در اتم های اکسیژن(مختصر بار منفی) و هیدروژن(مختصر بار مثبت) دارند، از بین این یون ها حرکت می کنند و جاذبه الکتروستاتیکی بین آن ها را از بین می برند.
مولکول های آب، یون ها را احاطه می کنند و به راحتی از هر نقطه محلول عبور می کنند. اگر ترکیبات یونی در محلول می توانند جریان الکتریکی را هدایت کنند، به دلیل آن است که یون های آزاد (که به راحتی حرکت می کنند)، باعث این کار شده اند.
برای این که حل شدن ترکیبات یونی را ببینید، شکل بالا را تماشا کنید. به این نکته دقت کنید که مولکول های آب چگونه خودشان را به اطراف یون های مختلف در محلول می رسانند.
حل شدن ترکیبات یونی در آب:
به نظر شما هنگامی که نمک طعام (NaCl) را در آب حل می کنید، تغییر فیزیکی اتفاق می افتد یا شیمیایی؟
یک تغییر فیزیکی منجر به تغییر در ظاهر ماده می شود اما هیچ ماده شیمیایی جدیدی در این تغییر به دست نمی آید. اما در تغییر شیمیایی، یک واکنش شیمیایی اتفاق می افتد و ماده جدیدی که نتیجه تغییر شیمیایی است، به دست می آید.
هنگام حل کردن نمک در آب، یون های مثبت و منفی آن به صورت زیر از هم جدا می شوند:
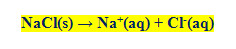
بنابراین حل شدن نمک در آب، مثالی از تغییر شیمیایی است.
البته برای جواب این سوال، اختلافات زیادی وجود دارد و برخی نیز معتقدند که حل شدن نمک در آب، تغییر فیزیکی است؛ چون اگر آب این محلول نمکی را بجوشانید، نمک به دست می آید. و این یک آزمایش ساده برای این است که به ماده اولیه می رسید یا نه.
نیروی جاذبه بین بارهای مخالف، یون هایNa+ و Cl- نمک را از هم جدا می کند.
هنگامی که مولکول های آب اطراف هر یون قرار می گیرند، لایه هیدرات (آب دار) اطراف هر یون نمک تشکیل می شود. این خاصیت جدید باعث می شود یون های Na+ و Cl- دوباره نتوانند با هم ترکیب یونی قبل از انحلال را تشکیل دهند.
در این حالت است که گفته می شود " نمک، حل شده است".
فرمول نويسي يک ترکيب يوني دو تايي را مي توان در سه مرحله ملاحظه کرد . براي نمونه به نوشتن فرمول شيميايي آلومينيوم اکسيد توجه کنيد:
۱) در اين اکسيد نماد کاتيون +۳Al و نماد آنيون ۲+ o است .
۲) نخست نماد کاتيون و سپس نماد آنيون را مي نويسيم ۲-Al+۳ o
۳) کوچکترين مضرب مشترک بارهاي اين دو يون برابر ۶(= ۳×۲)است . براي داشتن ۶ بار مثبت بايد ۲ يون +۳Al و براي ۶ بار منفي بايد ۳ يون ۲- o داشته باشيم. از اين رو نسبت o -۲ Al+۳ برابر ۲ به ۳ و فرمول شيميايي اين ترکيب به صورت Al۲ o۳ است.
نحوه شناسایی پیوندهای یونی و کوولانسی
الف. از طریق اختلاف الکترونگاتیوی :
از 0 تا 0.4 : کوالانسی ناقطبی
از 0.4 تا 1.7 : کوالانسی قطبی
از 1.7 تا 3.3 : پیوند یونی
ب. از طریق بعضی روش های تست زنی :
1.ترکیب یونی بین فلز و نافلز ایجاد میشود
شناسای فلز از نافلز هم که خیلی راحته . گوشه چپ جدول تناوبی عناصر قلیایی و قلیایی خاکی , وسط و پایین جدول فلزات واسطه سمت چپ جدول نافلزات و گازهای نجیب و هالوژن ها
2. ترکیب یونی بین یک کاتیون و آنیون ایجاد میشود.
باید تمام کاتیون ها و آنیون های تک اتمی و چند اتمی رو که در شیمی 2 فصل 3 نوشته شده حفظ باشین
3. Be و B یون تشکیل نمیدهند
4. ترکیبات C و Si کوالانسی است
5. آلومینیوم فقط با F , O و آنیون های اکسیژندار ترکیب یونی تشکیل میدهد
6. هر ترکیبی دارای یون NH4 باشد یونی است . این ترکیب علاوه بر پیوند یونی پیوند کوالانسی و داتیو نیز دارد.
پایان / موفق باشید
