مادون به معنای زیردست و بسیار ریز است لذا مادون قرمز اشعه بسیار ریز و قرمز رنگ می باشد . در سال ۱۸۰۰ میلادی سرویلیام هرشر یک نمونه نامرئی از تشعشعات را کشف کرد که این نمونه دقیقاً ناحیه قرمز طیف مرئی قرار داشت او این شکل از تشعشعات را مادون قرمز نامید . نور مرئی و پرتوهای مادون قرمز دو نمونه اشکال فراوانی از انرژی هستند که توسط تمام اجسام موجود در زمین و اجرام آسمانی تابانده می شوند . تنها با مطالعه این تشعشعات است که می توان اجرام آسمانی را تشخیص دهیم و تصویر کامل از چگونگی ایجاد جهان و تغییرات آن بدست آوریم .
دید کلی
تقریبا تمامی ترکیباتی که پیوند کوالانسی دارند، اعم از آلی یا معدنی ، فرکانسهای متفاوتی از اشعه الکترومغناطیسی را در ناحیه مادون قرمز طیف ، جذب میکنند. ناحیه مادون قرمز طیف الکترومغناطیسی ، دارای طول موجی بلندتر از طول موج نور مرئی (با طول موج تقریبی nm 800 - 400) و کوتاهتر از طول موج مایکروویو (باطول موج بلندتر از 1mm) است.
در شیمی ، ما فقط به بخش ارتعاشی ناحیه مادون قرمز علاقمندیم. این بخش ، طول موجی بین 2.5 μ را شامل میشود.
مانند انواع دیگر جذب انرژی ، موقعی که مولکولها ، اشعه مادون قرمز را جذب میکنند، به حالت انرژی بالاتر برانگیخته میگردند. جذب تابش مادون قرمز مانند هر فرآیند جذب دیگر ، یک فرآیند کوانتایی است، بدین صورت که فقط فرکانسهایی مشخص از تابش مادون قرمز توسط مولکول جذب میگردد. جذب تابش مادون قرمز با تغییر انرژی بین (KJ/mol (8-40 همراه است.
تابشی که دارای چنین انرژی باشد، فرکانسهای ارتعاشی کششی و خمشی پیوندهای کوالانسی اکثر مولکولها را شامل میگردند. در فرآیند جذب ، فرکانسهایی از اشعه مادون قرمز که با فرکانسهای ارتعاشی طبیعی مولکول مورد نظر تطبیق کند، جذب خواهد شد و انرژی جذب شده برای افزایش دامنه حرکت ارتعاشی اتصال موجود در مولکول بکار گرفته میشود. باید توجه داشت که تمامی پیوندهای موجود در مولکول ، قادر به جذب انرژی مادون قرمز نیستند، حتی اگر فرکانس اشعه ، کاملا با فرکانس حرکت تطبیق کند.
فقط آن پیوندهایی که دارای گشتاور دو قطبی هستند، قادر به جذب انرژی مادون قرمز خواهند بود. پیوندهای متقارن ، مثلا پیوند موجود در H2 و Cl2 ، اشعه مادون قرمز را جذب نمیکنند. یک پیوند باید خصلت یک دوقطبی الکتریکی را از خود بروز دهد که این دوقطبی با همان فرکانس اشعه ورودی متغیر است تا انتقال انرژی صورت پذیرد. بنابراین پیوندهای متقارن در مادون قرمز جذب نمیدهد.
اکثر پیوندهایی که چنین پدیدهای را دارند، پیوندهای موجود در آلکنهای متقارن و در آلکینهای متقارن هستند.
می توان گفت که تقریباً تمامی ترکیباتی که پیوند کووالانسی دارند، چه این مواد آلی باشند یا معدنی، فرکانس های متفاوتی از اشعه ی الکترومغناطیس را در ناحیه ی مادون قرمز طیف جذب می کنند.
ناحیه ی مادون قرمز طیف الکترومغناطیس دارای طول موجی بلندتر از طول موج نور مرئی است.
{ با طول موج تقریی m ) 400nm – 800 nm ) }
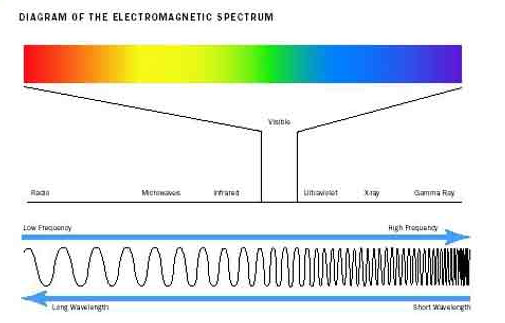
بخشی از طیف الکترومغناطیس را که ارتباط مادون قرمز ارتعاشی با دیگر تابش ها را نشان می دهد کوتاه تر از طول موج مایکروویو ( با طول موج بلندتر از 1mm ) است، در قسمت بالا مشاهده می کنید.
در شیمی ما فقط به بخش ارتعاشی ناحیه ی مادون قرمز علاقمندیم. این بخش طول موجی بین 25 µ , 2/5 µ را شامل می شود. اگر چه واحد تکنیکی صحیح طول موج در ناحیه ی مادون قرمز طیف میکرومتر ( µm ) است ، ولی ما واحد رایج آن یعنی میکرون ( µ ) را در این فصل به کار خواهیم برد .
در شکل فوق دیده می شود که طول موج رابطه ی عکس با فرکانس دارد. همان گونه که مشاهده می شود ، انرژی رابطه مستقیمی با فرکانس دارد: E = h v ، که h ثابت پلانک است.
با استفاده از فرمول اخیر می توان مشاهده کرد که ناحیه ی اشعه x دارای بالاترین انرژی در طیف بود و این انرژی آن قدر زیاد است که قادر به شکستن اتصال در مولکول خواهد بود.
در انتهای دیگر طیف الکترومغناطیس، فرکانس های رادیویی انرژی بسیار اندکی دارند.
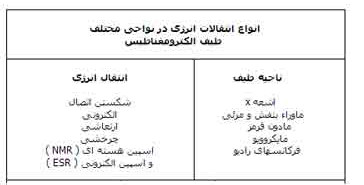
نواحی مختلف طیف و انواع انتقالات انرژی در جدول زیر خلاصه شده است. چندین ناحیه از جمله مادون قرمز، اطلاعات بسیار مهمی را در مورد مولکول های آلی در اختیار می نهند.
بسیاری از شیمیدانان از واحد عدد موجی ( میانگین رزونانس ) در ناحیه ی مادون قرمز طیف الکترومغناطیس استفاده می کنند . عدد موجی بر حسب cm -1 بیان شده است.
مزیت این واحد آن است که رابطه ی مستقیمی با انرژی دارد ( عدد موجی بیشتر نشانگر انرژی بیشتر است ) ، بنابراین، با استفاده از این واحد ، ناحیه ی ارتعاشی مادون قرمز بخشی بین 4000 تا cm -1 400 را در بر خواهد گرفت. می توان به کمک روابط زیر طول موج ( µM یا µ ) و عدد موجی ( cm -1 ) را به یکدیگر تبدیل کرد.
طیف سنجی مادون قرمز ، روشی برای شناسایی مولکولها و بخصوص گروه عاملی مولکولهاست. هر مادهای ، طیف مادون قرمز مخصوص به خود دارد و همانند اثر انگشت ، مختص خود مولکول میباشد. دستگاهی که طیف جذبی یک ترکیب را حاصل میکند، یک دستگاه طیف سنج مادون قرمز یا به عبارت دقیقتر یک اسکپتروفتومتر خوانده میشود.
دو نوع دستگاه طیف سنج مادون قرمز در آزمایشگاههای شیمی آلی بطور معمول مورد استفاده قرار میگیرد؛ دستگاههای تفکیکی (پراکندگی) و تبدیل فوریه (FT) .هر دو دستگاه ، طیفهای ترکیبات را در محدوده4000cm تا400cm فراهم میکنند. گرچه هر دو دستگاه ، طیفهای تقریبا یکسانی را برای یک ترکیب مشخص ارائه میدهند، ولی طیف سنج مادون قرمز FT ، طیف مادون قرمز را به مراتب سریعتر از دستگاههای تفکیکی تولید میکنند.
نور مادون قرمز:
اسپکتروفوتومتر مادون قرمز در شناسایی مولکولی و ارتعاشات وابسته به ساختار آن استفاده می شود. ساختارهای شیمیایی متفاوت، به دلیل تفاوت در انرژی های مربوط به هر طول موج، راههای مختلفی در پاسخ به طول موج های مختلف دارند. به عنوان مثال مادون قرمزهای برد متوسط، تمایل به لرزش دورانی دارد، درحالیکه مادون قرمز نزدیک (با انرژی بالاتر) تمایل به لرزش هارمونیک مولکولی مانند جنبش دارد.
در اسپکتروفوتومترهایIR متداول، یک پرتو مادون قرمز مستقیما به نمونه می تابد و تمام طول موجهای طیف نسبت به پرتو مرجع اندازهگیری میشود. به منظور تولید طیفی با کیفیت بالا، باید پهنای طیف ورودی به آرامی اسکن شود اسپکتروسکوپیIR با روش بسط تبدیل فوریه اصلاح می شود. قلب اسپکتروفوتومترهای IR تداخل سنج میشلسون است .
نور تابش شده از منبع IR به سمت سلولهای نمونه هدایت می شود. نیمی از پرتو تابشی از آینه ثابت باز تابیده شده و نیم دیگر آن از آینه ای که مرتبا در فاصله ای حدود دو و نیم میکرومتر حرکت می کند منعکس میشود. هنگامی که دوباره دو پرتو در آشکارساز با هم ترکیب می شوند و تداخل به وجود می آید، حدود دو ثانیه یک اسکن از فاصله ورودی گرفته شده و در کامپیوتر ذخیره می شود. به همین ترتیب چندین اسکن دیگر نیز به طور همزمان به آن اضافه می شود. با توجه به نوسانات و ارتعاشات حرارتی در آزمایشگاه بدیهی است که این امر نا ممکن است. پس به منظور حل این مشکل از لیزر هلیم – نئون برای تاباندن به تداخل سنج میشلسون استفاده می شود و تداخل لیزر به عنوان فرکانس مرجع به کار گرفته می شود.
استفاده از اسپکتروفوتومتر:
اسپکتروفوتومترها مستقیما برای اندازهگیری شدت نور در طول موج های مختلف استفاده می شود و میتواند نماینده درصد نور تابشی مخابره شده یا جذب شده باشد. با استفاده از این اطلاعات و مقایسه آن با دانسیتهها و دادههای به دست آمده میتوان اسپکتروسکوپی را به عنوان یک ابزار استفاده کرد. مقایسه طیفها برای تعیین غلظت جسم حل شده موجود در حلال مثال خوبی است. بدین ترتیب که با ثبت نور ارسال و دریافت شده در طول موجی خاص و بررسی طول موج جذب شده توسط حلال میتوان به غلظت آن پی برد. سپس آنالیز محلول با غلظت ناشناخته، با داده های معلوم مقایسه شده و به کمک تناسب ،غلظت محاسبه میشود. این عمل برای محلولهایی که در آنها چندین نوع حلال وجود دارد نیز قابل استفاده است والبته به دقت بیشتری در آنالیز طول موج ها احتیاج دارد. با توجه به حساسیت اسپکتروفوتومترFTIR مناسب ترین و رضایت بخش ترین روش آماده سازی نمونه، تبخیر ساده محلول نمونه در صفحه ای از نمک KBr و دست یافتن به طیفهای فیلم نازک باقی مانده است. این روش طیفی بسیار خوب با خط مبداء مسطح به وجود میآورد
اسپکتروفوتومترهایی که منبع نور ندارند اما طیفهای مبنی بر نور وارده را تولید می کنند میتوانند با روشی مشابه برای تعیین منبع نور استفاده شوند. میتوان منحنی طیفهای به دست آمده از منبع نوری نامعلوم (یا ترکیبی از منابع) را با اطلاعات منحنی های منبع نور مشخصی مقایسه کرد و منبع نور ناشناخته را شناسایی کرد.
از دیگر کاربردهای اسپکتروفوتومتر میتوان به تعیین ثابت موازنه واکنش های یونی که در محلولهای آبی انجام می شود اشاره کرد. در ابتدا طیفهای محلولی که تنها شامل یک واکنش دهنده است اندازهگیری می شود. سپس دیگر واکنش دهندهها به آن اضافه می شود و پس از هر بار افزایش، طیف سنجی صورت می گیرد. این روش در صورتی به صورت مطلوب کار می کند که طول موج جذب شده توسط محصول مقداری مشخص باشد. از آنجاکه بیشتر محصولات از اضافه کردن چندین واکنشگر به دست میآیند، زمانی که محلول اشباع شده و واکنش موازنه می شود نورهای بیشتری جذب شده و افزایش نور جذب شده برابر ثابت موازنه است
دستگاههای طیف سنج مادون قرمز تفکیکی
ساختمان و چگونگی ترسیم طیف:
یک طیف سنج مادون قرمز تفکیکی ساده از یک سیم داغ ، تولید اشعه مادون قرمز میکند که توسط دو آینه به دو اشعه موازی با شدت تابش یکسان تقسیم میگردد. نمونه در سر راه یکی از تابشها قرار گرفته و تابش دیگر بهعنوان شاهد بکار میرود. این تابشها سپس به تکفام ساز میرسند که هر تابش را بطور متناوب به یک شبکه پراش میفرستد.شبکه پراش به آهستگی میچرخد و فرکانس یا طول موج تابشی را که به آشکار کننده ترموکوپل میرسد، تغییر میدهد. آشکار کننده نسبت شدت بین تابش شاهد و تابش نمونه را تشخیص میدهد. بدین طریق ، آشکار کننده تعیین میکند که چه فرکانسهایی توسط نمونه جذب شده ، چه فرکانسهایی بوسیله نور عبوری از میان نمونه ، بدون تاثیر گذر کردهاند. پس از اینکه سیگنال حاصل از آشکار کننده تقویت گردید، ثبات طیف حاصل از نمونه را بر روی کاغذ ترسیم میکند.باید توجه داشت که طیف به گونهای که فرکانس تابش مادون قرمز با چرخش شبکه پراش تغییر مییابد، ثبت میگردد. گفته میشود که دستگاه های تفکیکی طیف را در قلمرو فرکانس ثبت میکنند. توجه داشته باشید که معمول است فرکانس (عدد موجی ،( cm-1 نسبت به نور عبوری (و نه نور جذب شده) ترسیم میگردد که دومی برحسب درصد عبور (T%) است. این بدین دلیل است که آشکار کننده نسبت شدت دو تابش را رسم میکند و:
=IsIr *100درصد عبور
که Isشدت تابش نمونه و Irشدت تابش شاهد است. در بعضی از نواحی طیف ، عبور ، تقریبا %100 است که نشان میدهد نمونه مورد آزمایش در آن قسمت از فرکانس اشعه ، شفاف است، یعنی جذبی صورت نمیگیرد. ماکزیمم جذب روی کاغذ با مینیمم عبور نشان داده میشود که حتی آن نیز قله خوانده میشود.
نقش حلال:
طیف یک ماده ، اغلب با حل کردن آن در یک حلال بدست میآید که بعد ، آن را در مقابل تابش نمونه در دستگاه قرار میدهند، در حالی که حلال خالصی در یک سلول معادل و در مقابل تابش شاهد قرار میگیرد. دستگاه بطور خودکار ، طیف آن حلال را از طیف نمونه مورد آزمایش کم میکند. همچنین ، این دستگاه اثرات گازهای جوی همچون انیدرید کربونیک و بخار آب را که در ناحیه مادون قرمز فعا ل بوده ، از طیف نمونه حذف مینماید (این گازها در معرض هر دو تابش وجود دارند).به همین دلیل است که بیشتر طیف سنجهای مادون قرمز ، دو تابشی (نمونه + شاهد) هستند و نسبت شدتها را اندازه میگیرند. چون حلال در هر دو تابش جذب میکند، لذا آن را در هر دو عبارت از نسبت IsIrوجود داشته و حذف میگردد. اگر یک مایع خالص (بدون حلال) ، مورد بررسی قرار گیرد، آن ترکیب فقط در محل تابش نمونه مستقر شده ، چیزی در محل تابش شاهد قرار نمیگیرد. هنگامی که طیف مایع بدست میآید، اثرات گازهای جوی بطور خودکار حذف میگردند، چون آنها در معرض هر دو تابش هستند.
طیف سنجهای تبدیل فوریه
ساختمان:
جدیدترین دستگاه های طیف سنج مادون قرمز با اصول متفاوتی کار میکنند. مسیر حرکت نوری به گونهای طراحی شده است که تولید طرحی میکند که تداخل نما نامیده میشود. تداخل نما یک سیگنال پیچیده است. ولی ، طرح موجی شکل آن ، شامل تمامی فرکانس هایی است که طیف مادون قرمز را میسازد. یک تداخل نما ، اساس نموداری از شدت نسبت به زمان (طیف قلمرو زمان) است.
اما یک شیمیدان ، بیشتر به طیفی که نموداری از شدت نسبت به فرکانس (طیف قلمرو فرکانس) خواهد بود، علاقمند است. یک عمل ریاضی که تبدیل فوریه (FT) خوانده میشود، قادر است فرکانسهای جذبی منفرد را از تداخل نما جدا نماید و در نتیجه طیفی معادل آنچه با طیف سنج تفکیکی بدست می آید، حاصل خواهد شد. این نوع دستگاه ، طیف سنج مادون قرمز تبدیل فوریه یا FT- IR خوانده میشود.
چگونگی ترسیم طیف:
دستگاههای FT- IR مرتبط به کامپیوتر ، با شیوه تک تابش کار میکنند. برای بدست آوردن طیف یک ترکیب ، شیمیدان ابتدا یک تداخل نمای "زمینه" را که شامل گازهای جوی فعال مادون قرمز همچون ایندرید کربونیک (CO2) و بخارآب (اکسیژن و نیتروژن غیر فعال مادون قرمز هستند) هستند، بدست میآورد. سپس تداخل نما تحت تبدیل فوریه قرار میگیرد که تولید طیف زمینه مینماید.
سپس شیمیدان ، ترکیب (نمونه) را در مقابل تابش اشعه قرار داده ، طیف حاصل از تبدیل تداخل نما را بدست میآورد. این طیف ، شامل نوارهایی برای ترکیب و زمینه است. نرم افزار کامپیوتر بطور خودکار ، طیف زمینه را از طیف نمونه کسر نموده ، طیف ترکیب مورد نظر را تولید مینماید. طیف کسر شده ، اساسا معادل با طیف بدست آمده از یک دستگاه تفکیکی دو تابشی قدیمی است.
مزیت دستگاه تبدیل فوریه به طیف سنج تفکیکی:
مزیت یک دستگاه FT- IR این است که آن تداخل نما را در کمتر از یک ثانیه حاصل میکند. پس ، میتوان تعداد زیادی از تداخل نماهای یک نمونه را جمع آوری کرده و در حافظه کامپیوتر ذخیره نمود. هنگام اجرای تبدیل فوریه بر روی مجموع تداخل نماهای جمع شده ، طیفی با نسبت سیگنال به نویز بهتر ترسیم میگردد. بنابراین یک دستگاه FT- IR سرعت و حساسیت بیشتری نسبت به دستگاه تفکیکی دارد.
چگونگی آماده سازی نمونه ها
نمونه جامد :
معمولا حدود 5 تا 15 میلی گرم نمونه را با حدود 400 میلی گرم برمور پتاسیم خالص و خشک مخلوط کرده ، بصورت پودر نرم و یکنواخت در آورده و با فشار زیاد بصورت یک قرص نازک و شفاف در می آوریم . KBr در طول موج 2.5 تا 25 میکرون جذب ندارد و این امکان میدهد که از نمونه طیف کاملی به دست آوریم. می توان از نمونه جامد به صورت سوسپانسیون ذرات بسیار ریز طیف گرفت . در این صورت حدود 5میلی گرم جسم را با یک قطره از Nujol ( یک هیدرو کربور اشباع شده پارافینی با وزن مولکولی بالا ) به صورت سوسپانسیون یکنواخت تهیه می کنیم .نوژول در نواحی 3030 – 2860 cm-1( بخاطر ارتعاشات کششی پیوند C-H) و همچنین در نواحی 1460 و 1374 cm-1(ارتعاشات خمشی پیوند C-H ) جذب دارد .وجود جذب در نوژول باعث می شود که اگر جسم در این نواحی جذب داشت ، تداخل ایجاد شود ، که در این صورت میتوان از هگزا کلرو بوتا دی ان استفاده کرد که فاقد پیوند C-H می باشد و در نتیجه میتوان جذب مربوط به C-H نمونه را مشاهده کرد.
نمونه مایع :
میتوان 2 قطره از مایع را بین دو سل کلرور سدیم قرار داد .اگر نمونه محلول حاوی حلال باشد ، چون همه حلالها در نواحی مختلف IR کم وبیش جذب دارند ، باید از حلال تنها به عنوان شاهد استفاده کرد .اگر نمونه با ويسکوزيته کم يا فرار باشد، از سلهای با ضخامت 0.1 میلی متر استفاده می شود .
نمونه گاز :
اگر نمونه به صورت گاز باشد از سل هایی که 10 سانتی متر طول دارد ،استفاده کرده و نمونه را به فضای آن تزریق می کنیم .
در هنگام نصب دستگاه اسپکتروفوتومتر باید به نکات زیر توجه داشت:
۱- اسپکتروفوتومتر باید روی سطحی سفت و در محیطی خشک و تمیز نصب شود.
۲- به جهت امکان جریان هوا در اطراف اسپکتروفوتومتر ، باید بین دستگاه و دیوارهای اطراف ۵۰ میلیمتر فاصله باشد.
۳- کابل برق دستگاه به پریز گراند شده با ولتاژ مناسب وصل شود.
۴- پس از اتصال آداپتورAC به برق، خروجی آن باید به گونه ای به دستگاه وصل شود که منبع ذخیرهDC در مسیر آن قرار گیرد.
۵- در صورتی که خود دستگاه فاقد پرینتر است، باید از طریق پورت مخصوص آنرا به پرینتر وصل کرد.
۶- پس از روشن کردن دستگاه مدتی صبر کرده تا دستگاه گرم شده و به پایداری حرارتی و الکترونیکی برسد.
کاليبراسيون:
برای کاليبره کردن دستگاه از فيلمهای پلی اتيلن يا پلی استيرن استفاده می کنيم که در نواحی خاصی پيک شارپ(تیز) دارند. بعنوان مثال اگر پيکی در 907 کاليبره است ودستگاه پيک رسم شده را در 905 داد. اختلاف را محاسبه کرده در مورد نمونه اعمال می کنيم. نکته قابل توجه اين است که در هر محدوده پيکها را بطور جداگانه بايد بررسی کرد.
پایان
